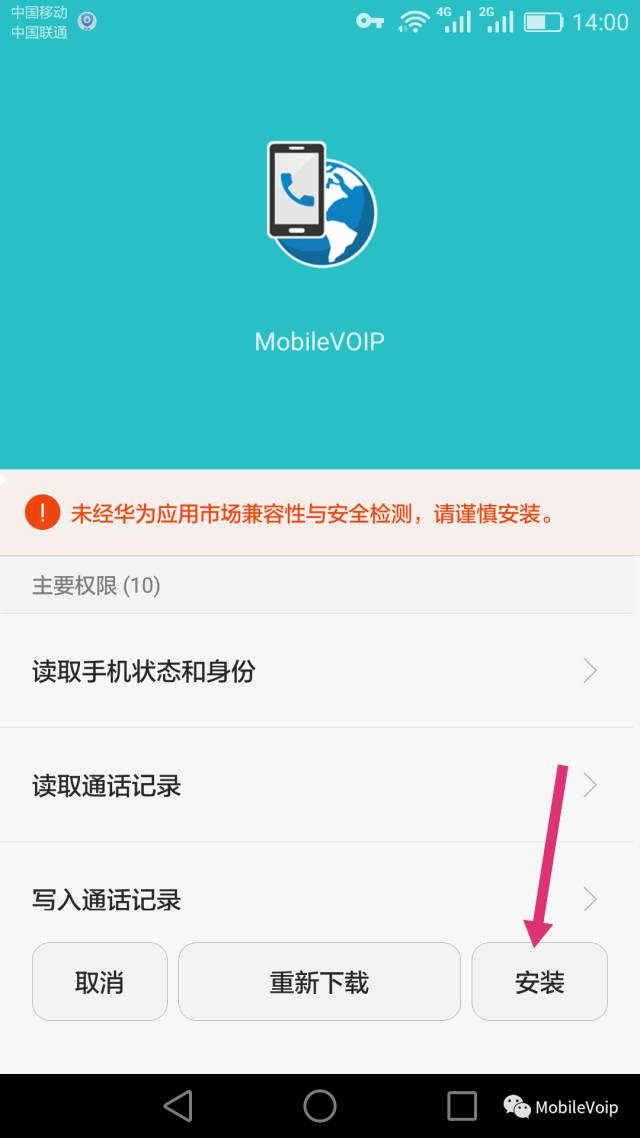
classin下载后打不开
˙▽˙ *** 次数:1999998 已用完,请联系开发者***
ˇ▂ˇ ...广生堂强调国产“First-in-class”乙肝创新药研发不确定性|速读公告是全球 First in class 的 MOA II 型乙肝核心蛋白抑制剂,是乙肝临床治愈的关键环节,专一性针对病毒靶点,对宿主靶点作用风险小,安全性高。目前全球尚无该靶点药物上市。 广生堂在乙肝治疗药物方面布局较为深远,除了GST-HG141之外,公司还布局了一、二代HBsAg抑制剂GST-HG131...
ˋωˊ 
out to lunch非常地道的“心不在焉”out to lunch 行为怪异;心不在焉; 疯狂的;神志不清的;过时的;懒散的;注意力不集中; behaving in a strange or confused way;如: You must have been out to lunch when you wrote that weird report. 当你做这个奇怪的报告的时候,你一定是神志不清的。 It seems that you were out to lunch in class. ...

21健讯Daily | 诺华超30亿美元总额收购Anthos公司;“核酸大王”张...药械审批强生两款first in class双抗在华获批上市2月11日,强生宣布锐珂(埃万妥单抗)和拓立珂(塔奎妥单抗)的上市申请均已获得国家药监局批准... 股,占公司总股本的0.0079%,不超过个人持股的25%。叶祥忠目前持有公司46.21万股,占公司总股本的0.0365%。更多内容请下载21财经APP

亿帆医药:F-652在研项目仍处后续研发与临床策略内部论证金融界1月16日消息,有投资者在互动平台向亿帆医药提问:请明确告知,F652研发项目是不是失败了?公司回答表示:F-652是公司在研1类原创生物药(First in Class),没有您所担心的情形,但作为原创新药后续存在开发风险大、投资大,甚至是最终研发失败的可能性。目前来看,F-652在研项目...
新股消息丨百利天恒港股IPO获中国证监会备案智通财经APP获悉,12月12日,中国证监会发布关于四川百利天恒药业股份有限公司境外发行上市备案通知书,公司拟发行不超过2427.1万股境外上市普通股并在香港联合交易所上市。据招股书,百利天恒于十年前的2014年,在美国西雅图创建了SystImmune、并开始研发first-in-class 的EG...
港股异动 | 石药集团(01093)涨超5% SYH2046片获中国临床试验批准智通财经APP获悉,石药集团(01093)涨超5%,截至发稿,涨5.12%,报5.54港元,成交额2.45亿港元。消息面上,4月11日,石药集团宣布,集团开发的SYH2046片已获得国家药品监督管理局批准,可在中国开展临床试验。该产品是一款具有完全自主知识产权的全新结构first-in-class小分子药物,本...
石药集团:SYH2046片获美国临床试验批准集团开发的化药1类新药SYH2046片已获得美国食品药品监督管理局(FDA)批准,可以在美国开展临床试验。该产品亦已于2025年4月获得中华人民共和国国家药品监督管理局批准,可以在中国开展临床试验。SYH2046片是一款具有完全自主知识产权的全新结构first-in-class小分子药物,本...

 ̄□ ̄|| 用于治疗间皮瘤!英硅智能泛TEAD抑制剂ISM6331获FDA的IND批件由生成式人工智能(AI)驱动的临床阶段生物科技公司英硅智能宣布,继2024年6月获得孤儿药认定(Orphan Drug Designation, ODD)后,公司自主研发的潜在“同类最佳”(best-in-class)泛TEAD抑制剂ISM6331于2024年7月获得美国食品药品监督管理局(FDA)的IND批件,用于治疗间皮瘤。使...

用于治疗间皮瘤!英矽智能泛TEAD抑制剂ISM6331获FDA的IND批件智通财经APP获悉,由生成式人工智能(AI)驱动的临床阶段生物科技公司英矽智能宣布,继2024年6月获得孤儿药认定(Orphan Drug Designation, ODD)后,公司自主研发的潜在“同类最佳”(best-in-class)泛TEAD抑制剂ISM6331于2024年7月获得美国食品药品监督管理局(FDA)的IND批件,用...
╯△╰ 
飞飞加速器部分文章、数据、图片来自互联网,一切版权均归源网站或源作者所有。
如果侵犯了你的权益请来信告知删除。邮箱:xxxxxxx@qq.com
上一篇:classin下载后打不开
下一篇:比特加速器






